第十三章 醫藥相關發明
1.前言
本章說明審查有關醫藥相關發明時,必須獨特判斷及處理之有關事項。適用本章之發明包括涉及醫藥用途之單一化合物、醫藥組成物、診斷或檢驗試劑、化妝品等醫藥領域之相關發明。
醫藥相關發明之審查,與其他章節共通之一般性規定,應參照其他章節。
本章所列舉之實例,僅係為說明本基準而設,並非說明書撰寫之範本,而且僅在所說明的特定議題上有其意義,不能據此推論該實例已經符合其他專利要件。
2.申請標的
2.1請求項之範疇
醫藥相關發明之請求項一般分為物之請求項及方法請求項。形式上為用途之請求項,其申請標的應視為相當於方法請求項。
2.1.1物之請求項
物之請求項,可包含下列態樣:
(1)化合物,例如「一種通式I化合物」、「一種通式I化合物及其鹽」、「一種化合物X之多晶型」。
(2)組成物,例如「一種醫藥組成物」、「一種用於治療C型肝炎之醫藥組成物」。
(3)劑型,例如「一種經皮吸收之貼劑」、「一種口服延長釋放錠劑」。
(4)套組,例如「一種偵測C型肝炎病毒之套組」、「一種治療哺乳動物肝腫瘤之藥學套組」。
(5)檢測裝置,例如「一種可攜式醫療檢測裝置」、「一種可利用近紅外線光譜分析進行非侵入性葡萄糖測定之設備」。
2.1.2方法請求項
(1)化合物之製備方法,例如「一種通式I化合物之製備方法」。
(2)組成物之製備方法,例如「一種醫藥組成物之製備方法」。
(3)劑型之製備方法,例如「一種製造口服延長釋放劑型之方法」。
(4)檢測方法,例如「一種肝臟疾病之篩檢方法」。
2.1.3用途請求項
(1)化合物或組成物用於製備藥物之用途,例如「一種使用請求項1之化合物於製造供治療睡眠失調症藥物之用途」。
(2)化合物或組成物用於醫療材料之用途,例如「一種含全氟烷基金屬錯合物用於作為斑塊、腫瘤及壞死組織成像MR造影之對比介質之用途」。
2.2法定不予發明專利之人類或動物之診斷、治療或外科手術方法
基於倫理道德之考量,顧及社會大眾醫療上的權益以及人類之尊嚴,使醫生在診斷、治療或外科手術過程中有選擇各種方法和條件的自由,若醫藥相關之方法發明係直接以有生命的人體或動物體為實施對象,則屬於人類或動物之診斷、治療或外科手術方法,為法定不予發明專利之標的。申請專利之發明係於活體外處理分離自人體或動物體之樣本(如血液、尿液、皮膚、毛髮、細胞或組織)的方法,或經由分析該樣本來收集資料的方法,原則上皆不屬於人類或動物之診斷、治療或外科手術方法。此外,自人體採取原料而於活體外製造醫療產物(例如血液製劑、疫苗、基因改造製劑等)或醫療材料(例如人體一部分的人工代用品或替代物,包括人造骨、經培育的皮膚片等)之方法,亦不屬於人類或動物之診斷、治療或外科手術方法。
2.2.1人類或動物之診斷方法
人類或動物之診斷方法,包括取得數據至作出診斷的所有步驟,亦即包括檢測有生命之人體或動物體(即測定實際值)、評估症狀(即比較測定值與標準值之差異)及決定病因或病灶狀態(推定前述差異所導致的診斷結果)的整個步驟過程,據以瞭解人類或動物之健康狀態,掌握其病情之方法。因此,診斷方法必須包含三項條件,始屬法定不予發明專利之標的,即(1)該方法係以有生命的人體或動物體為對象、(2)有關疾病之診斷及(3)以獲得疾病之診斷結果為直接目的。
上述所稱「以有生命的人體或動物體為對象」,係指該方法必須在有生命的人體或動物體上實施檢測或處理,即與人體或動物體產生交互作用(interaction),例如經由超音波來診斷心臟疾病之方法。反之,若僅係將取自人體或動物體的樣本於活體外實施檢測或處理,例如使用微陣列(microarray)分析血液樣本以診斷結腸癌,則不屬之。判斷一方法是否係「以有生命的人體或動物體為對象」,必須判斷該方法之步驟是否與人體或動物體產生交互作用,該交互作用的型態或強度並非是決定性的,只要該方法的實施(不包括醫生決定病因或病灶狀態之心智活動)必須有活體的存在,即屬之,不需要該方法與活體有直接接觸,例如一種評估即時肺部功能之方法,其包括於一個以上的呼氣階段之呼出氣體樣本中,測量一氧化氮含量及/或該一氧化氮含量的時間分布,雖然該測量係於脫離人體之呼出氣體執行,惟由於「於一個以上呼氣階段…測量…」之技術特徵,代表需要活體的存在且必須連接到儀器,故係「以有生命的人體或動物體為對象」。
上述所稱「有關疾病之診斷」,係指該方法必須與疾病之診斷有關,與疾病之診斷無關之方法或僅是量測人類或動物特性之方法,例如測量身高、體重或測定膚質等方法,均不屬於法定不予發明專利之標的。
上述所稱「以獲得疾病之診斷結果為直接目的」,係指該方法必須能獲得疾病之具體最終診斷結果。若申請專利之方法的直接目的並非診斷疾病者,而是從活體取得資訊(數據、物理量等),例如血壓量測方法、使用CT掃描成像的方法、測量血液中葡萄糖含量的方法等,其所獲得之資訊僅為中間結果,無法直接獲知疾病之診斷結果者,不屬於法定不予發明專利之標的。然而,若從有生命之人體測得某生理參數之方法發明,雖然其形式上並非以獲得疾病診斷結果為直接目的,但若依據先前技術中的醫學知識及該專利說明書揭露之內容,就該參數即能直接得知疾病之診斷結果者,則該發明不得稱為僅獲得診斷之中間結果,仍屬法定不予專利之人類或動物之診斷方法。
判斷申請專利之發明是否屬於人類或動物之診斷方法,與該方法是否符合上述定義有關,而與由誰來執行該方法或是否需要醫生在場或負責無關。
例1.
〔申請專利範圍〕
一種偵測人類是否患有腎臟疾病的方法,包括下列步驟:
(1)由疑似患有腎臟疾病之病人取得尿液樣本;
(2)於活體外測定抑制劑蛋白質X在該樣本內的濃度;及
(3)比較在步驟(2)測得之濃度,及正常人尿液中抑制劑蛋白質X的濃度。
(4)若該尿液樣本之抑制劑蛋白質X的濃度遠低於正常濃度,則表示患有腎臟疾病之可能性。
〔說明〕
申請專利之方法雖然包含從取得測量數據至做出診斷的所有步驟,但該方法係將由病人取得之樣本於活體外進行檢測,並非直接以有生命的人體為對象,故非屬人類或動物之診斷方法。
例2.
〔申請專利範圍〕
1.一種生物體之造影方法,該方法包括:
(1)施加一直流磁場於該生物體以磁化該生物體;
(2)提供一振動波至該生物體使該生物體振動,其中該振動波為音波或超音波;
(3)掃描該生物體的一磁特性變化;以及
(4)依據該生物體的該磁特性變化,產生相關於該生物體的一磁性造影影像。
〔說明〕
說明書雖然揭露該方法係以直流磁場及振動波的整合激發場進行磁特性感測以產生磁性造影影像,然後作為後續診斷及醫療上的參考,惟申請專利之方法僅限於檢測階段,缺乏評估症狀及決定病因或病灶狀態之後續步驟,即並無將取得數據與標準值比較以找出任何重要偏差以及推定前述差異所導致之診斷結果的步驟,故並未包含從取得測量數據到做出診斷的所有步驟,非屬人類或動物之診斷方法。
2.2.2人類或動物之治療方法
法定不予發明專利之人類或動物之治療方法,係指使有生命之人體或動物體恢復健康或獲得健康為目的之治療疾病或消除病因的方法,尚包括以治療為目的或具有治療性質的其他方法,例如預防疾病的方法、免疫的方法。此外,舒解或減輕疼痛或功能喪失等症狀的方法亦屬之,例如針對上癮或戒毒過程中產生盜汗、噁心等症狀的處理方法。申請專利之發明是否屬於人類或動物之治療方法,其判斷原則與診斷方法不同,只要方法中某一個步驟之技術特徵是用於治療疾病且實施於有生命之人體或動物體上,即使該方法尚包含其他非治療之步驟,該方法發明仍屬於人類或動物之治療方法。
2.2.2.1請求項涵蓋治療及非治療方法
若申請專利之方法可能涵蓋法定不予專利之治療方法及可准予專利之非治療方法,例如,請求項為「一種抑制凝血的方法,係將血液與含有化合物X及Y的載體接觸」,其範圍可能包括處理病人身體血液以作為治療方法的一部分(法定不予專利之標的),亦可能包括處理儲存於瓶中之血液的非治療方法(可准予專利之標的),因此仍屬人類或動物之治療方法而應不予專利。惟若由說明書之描述,可明確瞭解所請方法同時包含非治療方法,則應通知申請人於請求項中明確限定所請方法為非治療方法。例如請求項可修正為「一種處理儲存於瓶中之血液的方法,其包括將血液與含有化合物X及Y的載體接觸,以抑制凝血」。
審查時應注意申請專利之方法是否同時產生治療及非治療效果,若該方法產生之治療效果與非治療效果係無可避免地連結而無法區分,或是該非治療效果僅係治療效果的伴隨結果,則申請專利之方法仍屬法定不予專利之治療方法。反之,若申請專利之方法雖同時產生治療及非治療效果,然而該治療及非治療效果能夠明確區分,且於請求項中明確限定其係用於非治療之目的者,則非屬法定不予專利之治療方法。以下列舉常見涉及治療及非治療方法之態樣。
(1)口腔照護之方法
若申請專利之方法為「一種利用化合物X以去除牙菌斑的方法」,說明書雖然揭露該方法具有去除牙菌斑而改善牙齒外觀的美容效果,惟若使用化合物X用於去除牙菌斑時,無可避免地同時產生預防蛀牙及牙齦疾病的治療效果,且該二種效果無法區分,則屬於人類或動物之治療方法。
(2)單純之美容方法
若申請專利之發明係為以組合物A施用於有生命的人體或動物體之單純美容處理方法,例如使毛髮及指甲強化或避免毛髮減少的美容方法,非屬人類或動物之治療方法。此外,去除因老化而產生之皺紋的美容方法,由於去除因老化而引起的皺紋不具治療性質,亦非屬法定不予專利之治療方法。
(3)舒解或減輕疼痛等症狀之方法
舒解或減輕疼痛或功能喪失等症狀的方法,因其具有治療性質,故屬於法定不予專利之治療方法,例如針對上癮或戒斷過程中產生盜汗、噁心等症狀的處理方法。
(4)治療肥胖症之方法及減重之方法
一種減輕體重的方法或改善身體外觀之方法」,雖然可能包括用於美容性減重之非治療效果及用於治療肥胖症之治療效果,惟若請求項記載之技術特徵在於針對特定族群或使用特定劑量範圍,而使其產生的效果僅為美容性減輕體重而非治療肥胖症,二種效果可以明確區分,則非屬法定不予專利之治療方法。
(5)流產、避孕、及不孕症治療之方法
人工流產、終止妊娠或引產的方法屬法定不予專利之治療方法。原則上,一般的避孕方法不屬於人類或動物之治療方法,因懷孕本身不是一種疾病,惟若以治療為目的之避孕方法或是避孕方法伴隨有不可區分的治療效果,則屬於人類或動物之治療方法。例如,一種避孕方法,包含服用為了避孕目的之化合物A及為了預防因服用化合物A所產生副作用之化合物B,雖然服用化合物A非屬治療目的,然而服用化合物B涉及減輕症狀之治療目的,故該方法之整體仍屬人類或動物之治療方法。治療不孕症之方法,縱使包含體外受精之步驟,整體而言仍屬於法定不予專利之治療方法。
(6)使用移植儀器之方法
申請專利之方法的技術特徵雖然是直接作用在非活體標的物,例如植入物,惟若該方法可經由植入物對活體產生治療之目的或效果,則屬於人類或動物之治療方法。例如,一種操作心臟節律器的方法,若其特徵係調整心臟節律器以控制心臟對血液的輸出量,則屬於治療方法。反之,若該方法未對心臟產生刺激作用,僅是控制節律器之輸入能量,其目的是調整節律器能量消耗至最佳化,以減少該裝置的能量需求,但不影響對心臟的輸出能量,其特徵實質上是對植入物之一種技術操作,與該裝置在活體產生之治療效果並無功能上之關聯性,因此非屬法定不予專利之治療方法。
(7)於活體外進行處理之方法
人體或動物體的治療方法,雖實際上於活體外進行處理,但若該方法涵蓋返回生物體進行治療之步驟,仍屬法定不予專利之治療方法,例如活體外血液透析或過濾方法。
又例如,申請專利之方法為一種血液處理方法,係於離體(ex vivo)血液處理系統中添加抗凝血劑,或申請專利之方法為一種自血漿除去免疫球蛋白之方法,係於離體使用結合劑去除免疫球蛋白,若上述方法涵蓋該血液會返回患者,則屬於法定不予專利之治療方法。須注意者,從生物體分離之血液的處理方法,僅於申請專利之方法明確地或隱含地包括該血液返回至同一患者或動物體時,才屬於法定不予專利之治療方法。例如,一種從生物體分離之血液的處理方法,若請求項界定該血液以連續或「封閉迴路」(closed loop)過程返回至同一生物體,雖然請求項並未明確包括再輸注步驟(re-infusion step),該方法仍屬於治療方法。惟若申請專利之血液處理方法係於離體下進行且未涵蓋該血液之後續使用,不論儲存該血液係日後用於治療其他病人,或於日後治療同一病人,則非屬法定不予專利之治療方法。
例1.
〔申請專利範圍〕
一種保護人類皮膚免受UVA及UVB波長輻射作用之方法,包括局部施用一有效包覆之防曬組成物A。
〔說明〕
揭露防曬組成物A可保護人類皮膚免受UVA及UVB波長輻射作用,並可預防紅斑、老化症及皮膚癌。
〔結論〕
申請標的雖限定為「保護人類皮膚免受UVA及UVB波長輻射作用之方法」,非屬治療目的,惟說明書另揭露所請方法可用於預防紅斑、老化症及皮膚癌,係屬人類或動物之治療方法,而將此防曬組合物施用於皮膚時,除可達防曬之非治療效果外,同時亦可達到上述預防疾病之治療效果,且該二種效果無法區分,故所請方法屬於人類或動物之治療方法。
2.2.3人類或動物之外科手術方法
法定不予發明專利之人類或動物之外科手術方法,係指利用器械對有生命之人體或動物體實施剖切、切除、縫合、紋刺、注射及採血等創傷性或介入性之治療或處理方法。該方法有意地介入或破壞有生命之人體或動物體之生物體結構,包括近視雷射手術、牙科手術、內視鏡檢查、插入導管的方法及非以診斷、治療為目的之美容、整型(如割雙眼皮、抽脂塑身、豐胸)等方法。為外科手術而採用的預備性處理方法,例如皮膚消毒、麻醉等,亦屬於外科手術方法。若非以有生命之人體或動物體為對象而實施外科手術之方法,則不屬於法定不予專利之外科手術方法。
申請專利之發明是否屬於人類或動物之外科手術方法,其判斷原則與診斷方法不同,若申請專利之方法包含多個步驟,只要其中有一實施於有生命之人體或動物體之外科手術步驟,即使該方法尚包含其他非外科手術之步驟,仍屬法定不予專利之外科手術方法。
若申請專利之發明係以外科手術將某裝置植入或插入活體的方法,則屬於人類或動物之外科手術方法。惟若僅係操作植入裝置的方法,或是植入裝置與外部使用者或植入裝置與系統之間的交互作用方法,而該方法與裝置的植入方式無關,且不會作用於活體上,則非屬法定不予專利之外科手術方法。
例1.
〔申請專利範圍〕
一種心臟造影方法,該方法包括:
(1)將一具有心臟血流途徑之個體置於一磁振造影(MRI)系統,
(2)將極化之129Xe遞送至該個體上,
(3)於一標的區域沿著至少一個大角度無線電頻率刺激脈衝波之血流途徑,消溶(dissolve)一部分極化之129Xe,
(4)產生一結合刺激消溶極化129Xe之磁振造影。
〔說明〕
請求項之步驟(2)係「將極化之129Xe遞送到該個體上」,說明書記載該極化之129Xe係以注射或類似方法直接遞送至心臟區域,乃一種對活體施行之介入性的步驟,故步驟(2)係屬外科手術步驟,則申請專利之方法整體屬於人類或動物之外科手術方法。
2.3審查注意事項
(1)申請專利之發明是否構成法定不予專利之「人類或動物之診斷、治療或外科手術方法」,應就申請專利範圍之標的名稱是否為「方法」來判斷。以物為標的名稱之請求項,即使其用途係用於診斷、治療或外科手術方法,仍屬物之發明,非屬上述法定不予發明專利之方法,例如申請專利範圍之標的名稱為「醫藥組成物」或「套組」,均屬物之發明,即使所述之技術特徵涉及如使用劑量、給藥途徑、給藥間隔、不同成分先後使用等給藥方式,由於該等標的名稱非屬上述法定不予發明專利之方法,故不宜以專利法第24條第2款之規定予以核駁。
(2)申請專利之方法涵蓋治療方法及非治療方法,而申請時說明書未記載非治療方法之實施態樣,若將原請求項修正為限定於非治療方法者,則有超出申請時說明書、申請專利範圍或圖式之範圍,或無法為說明書所支持之問題。例如申請時說明書僅描述利用於人體產生抗雌激素效應以治療乳癌或不孕症之方法,並未描述其他非治療方法,則將請求項原載之「一種於人體產生抗雌激素效應的方法,…」修正為「一種於人體產生抗雌激素效應的方法,…但不包含治療方法」者,將導致請求項違反專利法第43條第2項或第26條第2項之規定。
(3)判斷是否屬於人類或動物之診斷方法,必須先確認請求項中是否包含從取得測量數據至做出診斷之全部步驟,若請求項中省略其中某一步驟,且該步驟對於該發明是必要的,則應以請求項未記載解決技術問題的所有必要技術特徵,無法明確且完整地界定申請專利之發明,以違反專利法第26條第2項之規定予以核駁。
3.說明書
3.1說明書之記載原則
說明書之記載應明確且充分揭露申請專利之發明,使該發明所屬技術領域中具有通常知識者在說明書、申請專利範圍及圖式三者整體之基礎上,參酌申請時之通常知識,無須過度實驗,即能瞭解其內容,據以製造及使用申請專利之發明,解決問題,並且產生預期的功效。
3.2可據以實現要件
審查人員必須依據申請時說明書揭露之內容,並參酌申請時之通常知識來判斷申請專利之發明是否無須經過度實驗即可據以實現該發明。評估是否必須過度實驗,應考量第一章1.3.1「可據以實現要件」所述之各項因素,包括申請專利範圍的廣度,申請專利之發明的本質,該發明所屬技術領域中具有通常知識者之一般知識及普通技能、發明在所屬技術領域中之可預測程度、說明書所提供指引的數量(amount of direction),包括先前技術中所述及者、基於揭露內容而製造及使用申請專利之發明所需實驗的數量。若該發明所屬技術領域中具有通常知識者在說明書、申請專利範圍及圖式三者整體之基礎上,參酌申請時之通常知識,須經過度實驗始能製造及使用申請專利之發明之全部範圍,則認定申請專利之發明違反可據以實現要件。
以下僅就醫藥產物、醫藥產物之製備方法及醫藥用途之特定事項加以說明。
3.2.1醫藥產物
醫藥產物發明包括以單一化合物(compound)、含有一種以上有效成分之組成物(composition)、含有二種以上有效成成分之組合(combination),或僅用結構及/或組成不能夠清楚描述之產物(例如植物萃取物)等作為醫藥有效成分者,其標的名稱可為化合物、組成物、組合,亦可為套組(kit)或包裝(package)等。以「組成物」為標的名稱者,係指其中成分混合使用。以「套組」或「包裝」為標的名稱者,其通常包含一種以上活性成分及實施該發明所需之必要元件。組合、套組或包裝,其中成分通常係同時或連續、或於特定時間間隔給藥。例如,一種有助於戒除煙草使用之套組,其含有化合物A及另一種有助於戒除煙草使用之活性成分B,其中該化合物A及該活性成分B在個別的分隔區內,並在相同或不同之包裝中,同時、分別或連續給藥。
申請專利之發明為醫藥產物者,說明書應記載醫藥產物的確認、製備及用途。由於醫藥發明所屬的技術領域,通常很難由其產物本身的結構來推論如何製造及使用該產物,故說明書通常必須記載一個或多個代表性實施方式或實施例,說明該產物如何被製造及如何被使用,以使該發明所屬技術領域中具有通常知識者能瞭解其內容並可據以實現該發明。
3.2.1.1產物之確認
關於化合物發明,說明書中應指明所請求之化合物,即應載明該化合物的化學名稱、結構式(包括各種官能基團、分子立體構型等)或分子式並應記載該化合物之物理、化學性質(例如各種定性、定量數據或光譜圖等),說明書之記載應明確且充分揭露至該發明所屬技術領域中具有通常知識者能確認該化合物的程度。
關於組成物發明,說明書應明確記載其組分,各組分可選擇的範圍及含量範圍,以及對組成物之性質或功能的影響,若有二種以上的活性成分,應記載其組成比例。組成比例之記載得以具體之用量或比例表示,包括重量、重量分、重量比例、重量百分比或其範圍等。組成物中若包含新穎之組分,應記載該組分之製造方法,使所屬技術領域中具有通常知識者能瞭解其內容並可據以實現。
對於僅用結構及/或組成不能夠清楚描述之產物為有效成分的發明,說明書中應提供其製備方法及使用至少一項足以確認該產物之特徵,例如進一步使用適當的物理、化學性質或其他特徵予以說明,使申請專利之產物能被清楚地被確認。醫藥產物之有效成分若涉及生物材料或中草藥萃取物者,說明書應記載事項參照第十四章4.「說明書」或第十五章3.2.3「萃取物」之相關規定。
3.2.1.2產物之製備
關於醫藥産物發明,說明書中必須記載至少一種製備方法,說明實施該方法所須之原料、製造步驟及條件(例如原料配合用量或比例、反應溫度、時間、壓力、pH值等)等。
3.2.1.3產物之用途
申請專利之發明為用於醫藥之化合物或醫藥組成物時,說明書中應記載其醫藥用途,例如所適用之病症或藥理作用,並記載其有效劑量及使用方法。若該發明所屬技術領域中具有通常知識者依據申請時之通常知識無法確認或推論該發明具有所主張之醫藥用途,則說明書應記載對該發明所屬技術領域中具有通常知識者而言,足以證明該發明所主張之醫藥用途的藥理試驗方法及結果。原則上,藥理試驗之記載必須包括進行該試驗所使用之方法及藥理試驗與發明所主張醫藥用途之關連性,以使該發明所屬技術領域中具有通常知識者能夠瞭解其內容並可據以實現。
上述進行藥理試驗所使用之方法,應包括所使用的化合物、使用劑量、給藥途徑、測試或分析方法或製劑方法、試驗結果等,其中藥理試驗結果通常應以數值資料記載,若無法以數值資料記載時,可提供一相當於數值資料之可接受的客觀評估記載,例如申請專利之發明為一種治療痤瘡之醫藥組成物,說明書記載施用該醫藥組成物於患者臉部,其皮膚紅腫及發炎反應已減輕之客觀評估結果。
藥理試驗應採用該發明所屬技術領域中具有通常知識者普遍採用的科學方法,例如活體外試驗、動物實驗或臨床試驗。
3.2.2醫藥產物之製備方法
申請專利之發明為化合物或醫藥組成物等醫藥產物之製備方法者,說明書應記載實施該發明之製備技術內容,包括原料、製程及產物。原料部分包括各個組分及配比(用量或比例)。製程部分包括製備步驟及參數條件(例如溫度、時間、pH值、使用之溶劑、催化劑、保護基團等)。
3.2.3醫藥用途
申請專利之發明為醫藥用途者,說明書應記載所使用之產物、醫藥用途(例如所適用之病症或藥理作用)、有效劑量及使用方法等,並應記載對該發明所屬技術領域中具有通常知識者而言,足以證明該產物可用於發明所主張醫藥用途之藥理試驗方法及結果。藥理試驗之記載方式參見本章3.2.1.3「產物之用途」。
3.3審查注意事項
(1)申請專利之發明經審查認為違反可據以實現要件時,審查人員應敘明該發明無法據以實現之理由,申請人得提出申復說明、相關文獻或與技術內容有關之補充說明或實驗結果等資料,以佐證根據說明書之記載,可使所屬技術領域具有通常知識者參酌申請時之通常知識,無須過度實驗,即能瞭解其內容,據以製造及使用申請專利之發明,惟不得於說明書中增加新的實施方式、實施例或實驗數據。
(2)申請專利之發明涉及醫藥用途時,原則上應提供對該發明所屬技術領域中具有通常知識者而言,足以證明該發明所主張之醫藥用途的藥理試驗方法及藥理試驗結果。若申請時說明書未記載任何藥理試驗之方法及藥理試驗結果,則違反可據以實現要件。即使申請人於接到審查意見通知之後另提出藥理試驗結果之書面資料,因申請時說明書未記載任何藥理試驗方法,申請日後所提出之藥理試驗結果,不能用以證明申請時說明書已明確且充分揭露該醫藥發明至該發明所屬技術領域中具有通常知識者能夠據以實現之程度,仍違反可據以實現要件。反之,若申請時說明書已詳細記載進行藥理試驗之具體方法,例如所使用之化合物、使用劑量、給藥途徑、測試或分析方法或製劑方法等,雖未記載藥理試驗結果或記載不完全,申請人為克服違反可據以實現之核駁理由,於申復說明時,提出含有藥理試驗結果之資料或相關文獻,審查時應注意該試驗是否使用與說明書記載內容一致的實驗方法,例如相同的化合物及藥理試驗方法,然該等資料僅可做為原揭露之發明確可據以實現之證明,不得載入說明書中。
(3)若說明書未載明用於藥理試驗之化合物,則無法確認申請專利之發明的藥理作用,例如申請時說明書中所述藥理試驗使用之化合物,僅記載「任何之本發明化合物」,但未具體指明是使用那一個化合物,則無法確認申請專利之發明的藥理作用,違反可據以實現要件。
3.4違反可據以實現要件之案例
例1.
該發明所屬技術領域中具有通常知識者依據說明書所揭露之內容,須過度實驗始能「製造」申請專利之發明
〔申請專利範圍〕
1. 一種可活化受體X之化合物,其係利用包含下列步驟之篩選方法而得:
(1)將候選化合物與可於細胞表面表現該受體X之細胞接觸,且
(2)判斷該候選化合物是否活化受體X。
2. 一種可抑制肥胖之醫藥組成物,包含可活化受體X之化合物作為活性成分,其中該化合物係由請求項1所述之篩選方法而得。
〔說明〕
說明書揭露一新穎受體X及篩選具有活化受體X功能之化合物的方法,並發現該化合物具有抑制肥胖之功效。說明書亦揭露篩選可活化受體X之化合物的細節,包括檢驗化合物是否可活化受體X之方法,並提供由該方法篩選得到可活化受體X之化合物A、B、C的實施例。說明書並揭露抑制肥胖之藥學機制理論及化合物A具有藥理效果之具體藥理試驗結果,但未記載除化合物A、B、C外之新穎化合物的化學結構特徵及製造方法。
〔結論〕
請求項1係以「可活化受體X」預期功能界定化合物,惟僅以所預期的功能界定化合物,通常難以確認或推論出具有該特定功能之化合物結構。說明書未提供化學結構等相關資訊,則可能使得該發明所屬技術領域中具有通常知識者須過度實驗始可製造眾多之化合物,並篩選出具有該特定功能之化合物。
該發明所屬技術領域中具有通常知識者雖可運用說明書所揭露方法進行化合物A、B、C之篩選,惟因說明書未揭露除化合物A、B、C外之其他活性化合物的相關資訊(例如化學結構),由化合物A、B、C之化學結構亦無法推論其他具有該特定功能之活性化合物的化學結構,即該等化合物之化學結構特徵與可活化受體X功能間之關係尚未知。因此,請求項1所請之化合物係以隨機篩選之方式而獲得,該發明所屬技術領域中具有通常知識者須過度實驗始可製造並篩選出具有該特定功能之化合物,不符合可據以實現要件。
請求項2係包含可活化受體X之化合物作為活性成分的醫藥組成物,雖然受體X係申請人首次發現,且可活化受體X之活性成分於申請時非屬該發明所屬技術領域之通常知識,然而說明書並未記載至該發明所屬技術領域中具有通常知識者能瞭解該活性成分為何之程度,該發明所屬技術領域中具有通常知識者須過度實驗始能篩選出具有特定功能之活性成分,不符合可據以實現要件。
例2.
該發明所屬技術領域中具有通常知識者依據說明書所揭露之內容,須過度實驗始能「使用」申請專利之發明(一)
〔申請專利範圍〕
一種成分A於製備止吐藥物之用途。
〔說明〕
說明書記載之成分A本身為已知化合物,申請專利之發明係發現成分A的新用途,然說明書並未記載成分A作為止吐劑之藥理試驗方法及藥理試驗結果,且依申請時之通常知識及申請時說明書記載之內容,無法確認或推論成分A具有止吐之功效。
〔結論〕
請求項係成分A作為止吐劑之用途,對該發明所屬技術領域中具有通常知識者而言,通常難以僅由化合物之名稱及化學結構來預測其醫藥用途。由於說明書未記載成分A作為止吐劑之藥理試驗方法及藥理試驗結果,該發明所屬技術領域中具有通常知識者無法僅由說明書記載之內容來確認該發明可用於該醫藥用途,即使考慮申請時之通常知識及說明書記載的作用機制等說明,亦無法推論成分A具有止吐之功效,因此,說明書並未明確且充分揭露,無法使該發明所屬技術領域中具有通常知識者能瞭解其內容並可據以實現,不符合可據以實現要件。
原則上,申請人於申復時補提成分A具有止吐功效之藥理試驗方法及藥理試驗結果的書面資料或實驗結果,並不能克服前述核駁理由,因「說明書應明確且充分揭露,使該發明所屬技術領域中具有通常知識者,能瞭解其內容並可據以實現」之判斷,係依據申請時說明書記載之內容。因此,若審查該說明書之記載內容,即使考慮申請時之通常知識,仍無法確認或推論成分A具有止吐之功效,雖於申請日後已確認之醫藥用途,仍不能證明申請時說明書已明確且充分揭露至該發明所屬技術領域中具有通常知識者能夠據以實現之程度。
例3.
該發明所屬技術領域中具有通常知識者依據說明書所揭露之內容,須過度實驗始能「使用」申請專利之發明(二)
〔申請專利範圍〕
一種疫苗,係由以下(a)及(b)所組成:
(a)由「Met-Ala-Ala……」胺基酸序列所組成之蛋白質A,
(b)一種(a)藥學上容許之載體。
〔說明〕
說明書具體記載(1)如何確認並分離出衍生自人類免疫不全病毒(HIV),且編碼含有「Met-Ala-Ala……」胺基酸序列之蛋白質A的DNA,(2)確認該DNA所編碼蛋白質A之表現並獲得該蛋白質A,(3)將該蛋白質A投予老鼠,可產生拮抗該蛋白質A之抗體,但是說明書並未記載拮抗蛋白質A之抗體中含有中和性抗體的存在,亦未提供蛋白質A作為疫苗功能之藥理資料。再者,由申請時之通常知識及申請時說明書記載之內容,無法確認或推論「衍生自HIV之蛋白質A」具有作為疫苗的功能。
〔結論〕
請求項係包含蛋白質A之疫苗,對該發明所屬技術領域中具有通常知識者而言,阻礙一物質活性之抗體即中和性抗體,必須辨識物質中僅少量存在之「中和性抗原決定位」,故可產生此種抗體之可能性通常很低,遑論尚未確定蛋白質A中是否存在「中和性抗原決定位」,要產生能辨識尚未確定是否存在於蛋白質A中之「中和性抗原決定位」的此種抗體之可能性應該很低,因此,說明書僅證明蛋白質A具有「免疫原性」是不足以證明其可作為疫苗之功能,必須證明「該抗體係藉由作用於蛋白質A之中和性抗原決定位之方式來阻礙HIV的活性」。由於說明書未具體記載蛋白質A作為疫苗功能之藥理資料,亦未記載拮抗蛋白質A之抗體具有中和HIV的活性,該發明所屬技術領域中具有通常知識者依申請時之通常知識及說明書記載之內容,無法確認或推論蛋白質A可作為疫苗的功能,因此,說明書並未明確且充分揭露,無法使該發明所屬技術領域中具有通常知識者能瞭解其內容並可據以實現,不符合可據以實現要件。
原則上,申請人於申復時提出蛋白質A具有疫苗功效之藥理試驗方法及藥理試驗結果之書面或實驗結
果,並不能克服上述之核駁理由,因為「說明書應明確且充分揭露,使該發明所屬技術領域中具有通常知識者,能瞭解其內容並可據以實現」之判斷,係依據申請時說明書記載內容,然說明書中對於由HIV衍生的蛋白質A可作為疫苗的功能並未記載至該發明所屬技術領域中具有通常知識者能夠確認或推論的程度,雖於申請日後已確認該功能,仍不能證明申請時說明書
已明確且充分揭露至該發明所屬技術領域中具有通常知識者能夠據以實現之程度。
例4.
該發明所屬技術領域中具有通常知識者依據說明書所揭露之內容,須過度實驗始能「使用」申請專利之發明(三)
〔申請專利範圍〕
一種通式(I)化合物於製備受體Z拮抗劑之用途,其中通式(I)化合物如下所示:
R-O-C6H4-CH(CH3)-COOH (I)
通式中,R代表氫、C1-C20烷基或含有1-3環的芳香基。
〔說明〕
說明書記載通式(I)化合物為已知化合物,申請專利之發明係發現通式(I)化合物作為受體Z拮抗劑的新用途,說明書並記載確認受體Z拮抗劑活性之藥理試驗方法及藥理試驗結果,其中僅有通式(I)化合物之取代基R為氫的藥理試驗結果。
〔結論〕
依申請時之通常知識已瞭解為了引進受體Z拮抗劑的拮抗活性,必須使鄰近伸苯基之氧鍵結在受體的相對點。此外,請求項之通式(I)化合物之取代基R的大小通常會影響受體Z之親和性,進而影響該化合物對受體Z之拮抗活性。據此,依申請時之通常知識,難以確認或推論即使通式(I)化合物取代基R之大小經改變,所導致對受體Z之拮抗活性仍然相同,且不能預期說明書通式(I)定義之所有化合物具有與實施例揭露的化合物相同之受體Z拮抗活性。
申請人於申復時若提出藥理試驗結果證實當通式(I)化合物之R係氫以外的取代基(須選擇較大的取代基)時,其受體Z拮抗活性與實施例中化合物之拮抗活性程度相同則可克服上述核駁理由。
此外,申請人亦可以申請時之通常知識為前提,提出書面意見敘明理由說明審查人員之核駁理由有誤,即引用先前技術文獻說明取代基R之大小對受體Z之拮抗活性並無影響,亦可克服上述核駁理由。
4.申請專利範圍
4.1請求項之範疇
醫藥相關發明請求項之範疇得區分為物之請求項及方法請求項。形式上為用途之請求項,例如「化合物A在治療胃病之用途」,應視同「使用化合物A在治療胃病之方法」,屬於方法發明。醫藥相關發明領域中,物之請求項包括化合物或其衍生形式(例如異構物、結晶物、水合物、溶劑合物等)、醫藥組成物、劑型(例如錠劑、栓劑及安瓿等)、套組、包裝或組合等申請標的。
以用途界定物之請求項,於解釋請求項時應當參酌說明書所揭露之內容及申請時之通常知識,考量請求項中的用途特徵是否對所請求保護之物產生影響,即該用途是否隱含請求保護的物具有適用該用途之某種特定結構及/或組成。若該用途之界定對所要求保護之物本身並無影響,僅係物之目的或使用方式之描述,對於申請專利之發明不具限定作用。
若申請專利之發明係關於將化合物或組成物用於人類或動物之診斷、治療或外科手術之目的,由於以用途(或使用、應用)為申請標的之醫藥用途請求項,視同方法請求項,因此請求項撰寫為「化合物A在治療疾病X之用途」,則視同「使用化合物A治療疾病X之方法」,屬於人類或動物之治療方法,應不予專利;若改以下列方式撰寫,例如、「化合物A在製備治療疾病X之藥物的用途」或「醫藥組成物B之用途,其係用於製備治療疾病X之藥物」等撰寫形式,則非屬法定不予發明專利之標的。其中,「化合物A在製備治療疾病X之藥物的用途」或「醫藥組成物B之用途,其係用於製備治療疾病X之藥物」等撰寫形式之醫藥用途請求項,稱為瑞士型請求項(Swiss-type claim),其申請標的視同一種製備藥物之方法,非屬人類或動物之治療方法。
涉及治療方法之方法請求項或用途請求項,例如「一種治療疾病X的方法,其係使用化合物A」或「化合物A用於治療疾病X的用途」,若修正為瑞士型請求項「化合物A用於製備治療疾病X之藥物的用途」,不視為超出申請時說明書、申請專利範圍或圖式所揭露之範圍。
此外,醫療器材、裝置或設備(例如手術儀器)並非「化合物」或「組成物」,其無法作為「製備藥物」之用途,因此亦不得以瑞士型請求項之撰寫方式申請新穎醫療用途(例如手術用途)。
由於瑞士型請求項之申請專利範圍視同一種製備藥物之方法,故即使其中之敘述涉及給藥方式,例如使用劑量、給藥途徑、給藥間隔、不同成分先後使用等,由於該申請標的非屬人類或動物之治療方法,故不宜以專利法第24條第2款之規定予以核駁。
4.2請求項之記載原則
發明專利權範圍,以申請專利範圍為準,申請專利範圍為申請專利之發明是否具備專利要件的審查對象。因此,申請專利範圍應界定申請專利之發明;其得包括一項以上之請求項,各請求項應以明確、簡潔之方式記載,且必須為說明書所支持,參見第一章2.4「請求項之記載原則」。
4.2.1明確
原則上,物之技術特徵應以結構予以界定,若無法以結構清楚界定時,始得以功能、特性、製法或用途予以界定,惟請求項之記載必須明確。參見第一章2.4.1「明確」。
4.2.1.1化合物請求項
申請專利之發明為化合物時,由於很難以化合物之功能或特性來預測其結構,原則上應以化學名稱或分子式、結構式等結構特徵界定其請求項。若無法以化學名稱或分子式、結構式界定時,得以物理、化學特性(例如熔點、分子量、光譜、pH值等)界定;若仍無法以物理或化學特性界定時,得以製法界定,惟請求項中應記載有別於先前技術之必要技術特徵,使該發明所屬技術領域中具有通常知識者足以認定該申請標的與先前技術之區別。此外,若有特殊之功能或用途,且足以顯示其技術特徵者,得加入該功能或用途之記載一併界定,但不允許僅以純功能或純用途界定化合物。原則上,化合物之名稱應當按通用的命名法來命名,不允許使用商品名或者代號,化合物之結構必須明確,不能用含糊不清的用詞。
對於化合物之衍生形式,例如藥學上可接受之鹽或酯、立體異構物、水合物等,若於說明書已明確記載該化合物具有衍生形式,且該發明所屬技術領域中具有通常知識者依據說明書關於該化合物之揭露,即可明瞭在無須過度實驗下製得該化合物之衍生形式者,得於化合物請求項中一併主張。
須注意者,於請求項中同時主張化合物及其藥學上可接受鹽或酯、異構物或水合物等衍生形式者,於相關附屬項應記載其所引用請求項之完整標的名稱,避免有不一致之情形。例如請求項1之標的名稱為「一種式(I)化合物及其藥學上可接受之鹽、異構物、水合物」,其附屬項應記載為「如請求項1之式(I)化合物及其藥學上可接受之鹽、異構物、水合物」。
申請專利之發明為「一種式(I)化合物及其衍生物,…」就發明所屬技術領域中具有通常知識者而言,無法瞭解所述衍生物為何種物質,導致請求項不明確。
例1.
〔申請專利範圍〕
一種式(I)化合物或其藥學上可接受鹽、對映異構物、水合物,
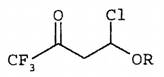 (I)
(I)
其中R選自C1-8烷基及苯基。
〔說明〕
申請時說明書中已記載式(I)化合物具有藥學上可接受鹽、對映異構物或水合物之衍生形式,若該發明所屬技術領域中具有通常知識者依據說明書關於式(I)化合物之記載,可明瞭在無須過度實驗下製得該等衍生形式,得於請求項1中一併主張。
例2.
〔申請專利範圍〕
1.一種式(I)化合物或其藥學上可接受鹽、對映異構物、水合物,
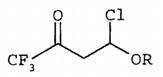 (I)
(I)
其中R選自C1-8烷基及苯基。
2. 一種製造如請求項1之式(I)化合物的方法,……。
〔說明〕
請求項2為引用記載形式,由於請求項2僅引用請求項1之部分申請標的(即式(I)化合物),解釋上,請求項2之製造方法不包含製造式(I)化合物之藥學上可接受鹽、對映異構物或水合物。
申請專利之發明為化合物之結晶物時,原則上,請求項應以具有其技術特徵之物理、化學特性,例如X射線粉末繞射、X射線單晶繞射、IR、Raman、NMR等光譜分析法、或DTA、TGA、DSC等熱分析方法之數值界定其晶體結構。請求項撰寫為「一種化合物X之結晶物A型」,因所述之結晶物A型是任意的名稱,並無技術特徵之描述,是不明確的。
4.2.1.2醫藥組成物請求項
醫藥組成物請求項應以組成物的組分或者組分及含量等組成特徵來表示,並使用適當之連接詞如開放式、封閉式及半開放式等表達方式,連接詞之表達方式與意義,參見第一章2.3.3「連接詞」。
組成物中各組分應以明確之用語界定,單純以功能性用語界定組分者,若所屬技術領域中具有通常知識者依據申請時之通常知識無法瞭解所界定組分之內容,請求項為不明確。
若發明之特徵或改良僅限於組分本身,即發明所欲解決的技術問題係選擇特定之組分,至於組分的含量乃該發明所屬技術領域具有通常知識者依據申請時之通常知識或以簡單實驗即能確定者,則請求項中可以僅界定組分。反之,若發明之特徵或改良非僅限於組分,且與含量有關,即發明所欲解決的技術問題不僅在於選擇特定之組分,且要確定該組分之特定含量,則請求項中應同時記載組分與含量,以明確界定其必要技術特徵。
若發明之特徵或改良在於醫藥劑型,例如「一種經皮吸收之貼劑」、「一種口服延長釋放錠劑」等,請求項中應同時界定特定有效成分及與所請劑型有關之必要技術特徵,例如賦形劑、配合用量等。單純以性質參數(例如溶解度)、藥物動力學或藥效動力學參數作為劑型之必要技特徵者,是不明確。
醫藥組成物請求項,若所述之醫藥用途僅以功能性用語或定義界定所欲治療的症狀,而該發明所屬技術領域中具有通常知識者無法瞭解所涵蓋的具體病症為何,原則上該請求項是不明確的,除非說明書提供實驗測試或測試標準之指示,或該發明所屬技術領域中具有通常知識者依據申請時說明書揭露之內容,並參酌申請時之通常知識可判斷該用語或定義對應於一個或以上的具體病症名稱,該請求項始為明確。例如請求項界定之病症為「任何可能藉由對特定受體選擇性佔有而改善或預防之病症」,然而,依據申請時之通常知識及申請時說明書揭露之內容無法瞭解具體之病症為何,則該請求項所界定之範圍不明確。
以「醫藥組成物」為申請標的者,若其中記載之技術特徵為給藥方式,例如同一成分間隔給藥、不同成分先後使用等,與標的之「組成物」不符,應視發明之實質技術內容而使用適當標的,如「組合」或「用途」。例如,申請專利之發明係關於「以化合物A來治療Y疾病,其特徵在於以化合物A之初始劑量為5.0至10.0 mg/kg給藥,停藥2天,再以2.0至5.0 mg/kg之劑量給藥3天,依序循環給藥」,則不宜以醫藥組成物作為申請標的,應改以瑞士型請求項之製備藥物「用途」作為申請標的,修正為「化合物A用於製備治療Y疾病之藥物的用途,其係以化合物A之初始劑量為5.0至10.0 mg/kg給藥,停藥2天,再以2.0至5.0 mg/kg之劑量給藥3天,依序循環給藥」。
申請專利之發明撰寫為「一種醫藥組成物,其包含化合物X以及一稀釋劑、賦形劑或載劑」。若該組成物之新穎技術特徵是化合物X,而稀釋劑、賦形劑或載劑可由該發明所屬技術領域中具有通常知識者來選擇或由一般性實驗來決定,則不須於請求項中進一步界定該稀釋劑、賦形劑或載劑之種類,該請求項係明確的。
原則上,請求項中以文字定性之敘述代替數字定量的表示方式,若其意義是清楚明確,且為該發明所屬技術領域中具有通常知識者所習知,則得以此類用語表現。例如,請求項中以「治療有效量」界定一新穎之活性成分的含量是明確的。反之,若以「治療有效量」界定一已知活性成分,而以該用語作為其與先前技術之唯一區分,由於無法界定請求保護之範圍,因此是不明確。
請求項中敘述產物的純度不能僅界定該物質是「作為一個醫藥產物」,應有具體的數值表示該純度,否則不明確。
4.2.1.3醫藥用途請求項
醫藥用途請求項中所述之醫藥用途應明確,得以所適用之病症名稱或藥理作用予以界定,例如「式I化合物用於製備治療糖尿病之藥物的用途」、「一種式I化合物的用途,其係用於製造抑制β-澱粉樣蛋白肽之釋出之醫藥組合物」。用以界定該新穎醫藥用途的用語必須明確,參見本章4.2.1.2「醫藥組成物請求項」。
若醫藥用途發明的特徵涉及給藥對象、給藥方式、途徑、使用劑量或時間間隔等,應於瑞士型請求項之記載形式中一併界定該等必要技術特徵,以明確界定其醫藥用途。
例1.
〔申請專利範圍〕
一種抑制肥胖的醫藥組合物,其係包含可活化受體X的化合物。
〔說明〕
說明書揭露一新穎受體X及篩選具有活化受體X能力的化合物之方法,並發現該化合物有抑制肥胖之功效。
說明書揭露篩選可活化受體X的化合物之細節,包括檢驗化合物是否可活化受體X之方法,並記載由該方法篩選得到可活化受體X之新穎化合物A、B、C的實施例,且確認A、B、C有活化受體X的功效。然而,未記載A、B、C以外之任何新穎化合物的化學結構或製造方法。
〔結論〕
由於受體X是申請人首次發現,考量申請時之通常知識,所屬技術領域者,無法推想出具有受體X活性作用之具體的化合物,因此,發明之範圍不明確。若申請人修正申請專利範圍,例如限定該化合物為A、B、C,而使該發明所屬技術領域中具有通常知識者,由請求項之界定內容,並參酌申請時之通常知識,即可確認具有受體X活化能力之新穎化合物,則可克服該核駁理由。
例2.
〔申請專利範圍〕
一種H2阻斷劑作為製備抗過敏劑之用途。
〔說明〕
說明書揭露關於一個習知H2阻斷劑的新穎用途,申請前之先前技術並未揭露H2阻斷劑具有抗過敏的功效。然而,申請時已知多種化合物可作為H2阻斷劑,例如希美替定(cimetidine)、雷尼替定(ranitidine)、啡莫替定(famotidine)及羅莎替定醋酸酯(roxatidine acetate)。
〔結論〕
請求項之「H2阻斷劑」雖然並未具體界定所包含之活性成分,然而依申請時之通常知識,可以瞭解「H2阻斷劑」之具體的活性成分為何,故該請求項之範圍是明確的。
4.2.2簡潔
簡潔之審查參見第一章2.4.2「簡潔」。
4.2.3為說明書所支持
有關化合物請求項,必須考慮該申請專利範圍是否得到說明書之支持,亦即基於說明書所揭露之內容,利用例行之實驗或分析方法是否足以將說明書揭露之內容合理預期或延伸到請求項之範圍,或對於說明書所揭露之內容是否僅作明顯之修飾即能獲致者。例如請求項為以具有眾多選擇項目的馬庫西型式(Markush-type)記載之化合物,若說明書中對於含有該選擇項目之特定結構的化合物,僅記載少數具體實施例,對於含有該選擇項目之其他結構的化合物,若基於說明書所揭露之內容及申請時之通常知識,並非利用例行之實驗方法或僅作明顯之修飾即能獲致者,則申請專利之化合物無法為說明書所支持。
有關醫藥組成物或醫藥用途請求項,若所請範圍涵蓋化合物及其衍生物,而說明書僅提供化合物本身醫藥用途之實施方式或實施例,未提供衍生物醫藥用途之實施方式或實施例,若因該發明所屬技術領域中具有通常知識者,無法僅由化合物之實施方式或實施例合理預期或延伸得知其他可能的衍生物均可以達到所主張之醫藥用途,則說明書之揭露不足以支持申請專利之發明。
有關醫藥組成物或醫藥用途請求項,若僅以功能界定一群化合物,例如一特殊受體之拮抗劑,則必須確認是否得到說明書之支持。若說明書僅例示某類功能性化合物中有一個化合物可用來治療某特定疾病,並不代表所有此類功能性化合物均可用來治療該疾病,除非有足夠證據證明該治療效果與該類化合物所具有之特定功能相關。
例1.
〔申請專利範圍〕
1. 一種具有阻礙IL-X作用之化合物於製備抗過敏藥物之用途。
2. 如請求項1之用途,其中具有阻礙IL-X作用之化合物為通式(I)所示之化合物。
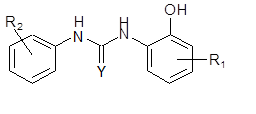
〔說明〕
說明書揭露具有阻礙IL-X作用之化合物作為抗過敏之醫藥用途,亦揭露通式(I)化合物,其中Y為氧原子或硫原子,R1及R2為分別從氫、鹵素、硝基、氰基及C1-6烷基中所選出者。實施例確認通式(I)化合物所包含之數個具體化合物具有抗過敏作用。然而,說明書並未揭露其他具有阻礙IL-X作用之化合物亦具有抗過敏作用之理論或實驗,依據申請時之通常知識亦未能確認具有阻礙IL-X作用之化合物具有抗過敏作用。
〔結論〕
請求項1係以「IL-X阻礙活性」之預期性質主張界定之化合物的抗過敏之醫藥用途,所請範圍涵蓋具有該性質之彼此結構不相似的任何化合物,但說明書僅揭露請求項2所界定之通式(I)化合物,其係請求項1所請範圍中之化合物的極少部分。再者,說明書僅確認請求項2之通式(I)化合物所包含之少數具體化合物具有抗過敏功效,並未揭露具有阻礙IL-X作用之其他化合物亦具有抗過敏作用的理論或實驗,該發明所屬技術領域中具有通常知識者,基於申請時之通常知識亦無法確認或推論其有效性,且非利用例行之實驗或分析方法即可合理延伸者,因此請求項1無法為說明書所支持。
例2.
〔申請專利範圍〕
一種化合物於製備治療腫瘤藥物之用途,該化合物係為一選自異喹啉生物鹼化合物A、B或C之硫酸鹽。
〔說明〕
化合物A、B及C為已知之具有異喹啉骨架結構的異喹啉生物鹼,且已知化合物A本身可作為治療腫瘤之藥物。說明書揭露將化合物A製備成其硫酸鹽時,可提升其治療腫瘤之功效,實施例中腫瘤動物模式之藥理試驗顯示,化合物A、B之硫酸鹽相較於化合物A之鹽酸鹽,具有提升之腫瘤治療效果。
引證1揭露化合物C之鹽酸鹽對於表現腫瘤之受試動物不具有治療功效,但並未說明化合物B之鹽酸鹽是否具有腫瘤治療效果。
〔結論〕
請求項雖明確界定治療腫瘤之藥物包含一選自異喹啉生物鹼化合物A、B或C之硫酸鹽作為活性成分,但說明書僅揭露化合物A、B之硫酸鹽具有腫瘤治療效果。而引證1揭露化合物C之鹽酸鹽不具有腫瘤治療效果,雖引證1未揭露化合物C之硫酸鹽,然對於該發明所屬領域中具有通常知識者而言,原則上由同一化合物製備而得之不同種類的鹽類產物彼此間具有相似之藥理作用,故可合理推論化合物C之硫酸鹽的藥理作用與化合物C之鹽酸鹽相似,亦不具有腫瘤治療效果。再者,說明書並未確認化合物C之硫酸鹽具有腫瘤治療效果,該發明所屬技術領域中具有通常知識者,基於申請時之通常知識及引證1,無法合理延伸至包含化合物C之硫酸鹽的範圍亦具有腫瘤治療效果,因此,請求項無法為說明書所支持。此外,說明書之記載未明確充分揭露,使該發明所屬技術領域中具有通常知識者參酌申請時之通常知識及引證1,無法據以實現申請專利之發明,不符可據以實現要件。
4.2.4審查注意事項
(1)有關醫藥用途請求項,若以藥理作用界定其所製備藥物之用途,則須該發明所屬技術領域中具有通常知識者,就該藥理作用參酌申請時之通常知識,可得實質對應一個或以上的具體病症名稱,始認定請求項為明確;否則,該請求項不明確,另可能亦有無法獲得說明書支持之問題。
(2)引用記載形式之請求項通常為附屬項,惟若存在與其所引用之請求項的範疇不同、標的名稱不同,或未包含其所引用之請求項中所有的技術特徵的情況時,審查人員應於審查意見通知中敘明,若申請人未修正,則該引用記載形式之請求項應解釋為獨立項。例如,獨立項請求項1之標的名稱為「一種式(I)化合物及其異構物、水合物,……」其附屬項請求項2應記載為「如請求項1之式(I)化合物及其異構物、水合物,……」,若僅記載為「如請求項1之式(I)化合物,……」則請求項2實質上應解釋為獨立項。
5.專利要件
5.1產業利用性
醫藥産物之發明,應於說明書中具體指明產物之醫藥用途,而非僅籠統說明該產物可能是有用的,例如說明書僅記載請求之化合物可用來治療未特定的疾病或該化合物具有有用的生物特性,不足以證明該發明具有產業利用性。中間體之產業利用性,係由其最終產物來認定,故必須記載最終產物之用途。
5.2新穎性
5.2.1化合物
申請專利之發明為一種化合物,若引證文件已經載明一化合物的(i)化學名稱、(ii)分子式(或結構式)、(iii)理化參數等性質及/或(iv)一種製備方法(包括原料),該發明所屬技術領域中具有通常知識者,依該文件的揭露內容及結合申請時之通常知識,能夠製造或分離出該化合物,則該化合物不具新穎性。惟若引證文件中僅說明其存在或提到其名稱或化學式,而未說明如何製造及使用該化合物,且該發明所屬技術領域中具有通常知識者無法從該文件內容或文件公開時可獲得之通常知識理解到如何製造或分離該化合物,則不能依該文件認定該化合物不具新穎性。
原則上,上位概念發明之公開不影響下位概念發明之新穎性,故引證文件所揭露化合物之化學通式不會使申請專利之該通式中的一個具體化合物喪失新穎性,例如低碳烷基(lower alkyl)之揭露不會使乙基(C2H5)喪失新穎性。反之,若先前技術為下位概念發明,且其內容已隱含或建議其所揭露之技術手段可以適用於其所屬之上位概念發明,則下位概念發明之公開會使其所屬之上位概念發明喪失新穎性,例如一個具體化合物的公開會使包括該具體化合物之通式的請求項喪失新穎性,但不影響該通式所包括除該具體化合物以外之其他個別化合物的新穎性。以用途界定化合物之請求項,通常只是對該物的用途或使用方法的描述,應認定其申請專利範圍為化合物本身,而不具有用途之限定。例如,「用於殺絛蟲」僅是表示化合物之用途,因此,「用於殺絛蟲之化合物A」與未界定用途之已知化合物A並無不同,故「用於殺絛蟲之化合物A」不具新穎性。
5.2.1.1異構物、水合物、溶劑合物或結晶物
化合物A雖已公開於引證文件,若引證文件之內容並未揭露至該發明所屬技術領域中具有通常知識者能製造及使用其異構物、水合物、溶劑合物或結晶物之程度,則其異構物、水合物、溶劑合物或結晶物具有新穎性。
申請專利之發明為一已知化合物之對映異構物(enantiomer),若引證文件公開該化合物之外消旋混合物(racemic mixture),但並未具體公開各種光學異構物,雖然實際上,該化合物的各種光學異構物係客觀存在,只是未個別單離出來,然而因引證文件之內容並未揭露至該發明所屬技術領域中具有通常知識者能製造及使用該對映異構物之程度,則申請專利之發明具有新穎性。
若引證文件不僅公開一外消旋混合物,且引證文件記載製備該對映異構物的原料及方法,足以使該發明所屬技術領域中具有通常知識者能製造及使用該對映異構物,則該對映異構物不具新穎性。
5.2.1.2化合物之選擇發明
選擇發明係由先前技術已知之較大的一個群組或範圍中,選出其中未特定揭露之個別成分(individual element)、次群組(sub-sets)或次範圍(sub-ranges)之發明,其他規定另參照第三章2.5.4「選擇發明」。
判斷化合物之選擇發明的新穎性時,必須判斷所選出的化合物是否於先前技術中已以個別具體的形式被揭露。
若申請專利之化合物中特定取代基係自先前技術之化學通式中單一取代基群組中所選出者,則不具新穎性,例如先前技術揭露某化合物X之化學通式,其中取代基R1為COOH,取代基R2為選自Cl、SO3H、CH3、……、CH2CH2CH3之基團,若申請專利之發明為取代基R1為COOH且取代基R2為CH2CH2CH3之化合物,因該具體之化合物已公開於先前技術,故不具新穎性。然而,若申請專利之化合物係從先前技術中特定範圍之二個以上之取代基群組中分別選出特定取代而產生者,其係為了達成特徵的特定組合且該組合並未特定具體地揭露於先前技術中,則具有新穎性,例如先前技術揭露通式化合物X,其中取代基R1為COOH、NH2、……、苯基之基團,取代基R2為選自Cl、SO3H、CH3、……、CH2CH2CH3之基團,若申請專利之發明為取代基R1為COOH及取代基R2為CH2CH2CH3之化合物,因先前技術並未具體揭露自R1與R2之眾多選項中特定選出取代基COOH及CH2CH2CH3組合而產生之該個別化合物,則具有新穎性。
5.2.2醫藥組成物
醫藥組成物之技術特徵若為具有特定藥理作用的一個或一群化合物,判斷醫藥組成物的新穎性主要就該一個或一群化合物來考慮,例如申請專利之醫藥組成物與先前技術揭露之醫藥組成物相較,若其中具有特定藥理作用之一個或一群化合物不同,則所請醫藥組成物發明具有新穎性。此外,若醫藥組成物之技術特徵包含具有特定藥理作用之一個或一群化合物、不具有特定藥理作用之其他組分(例如填充劑、崩解劑等)以及組分含量或用量比例等,該醫藥組成物與先前技術揭露之醫藥組成物相較,只要有一個技術特徵不同,則該醫藥組成物具有新穎性。
有關以醫藥用途界定組成物之發明,通常只是對該組成物所適用之病症、藥理作用或使用方法的描述,應認定其請求項所請為組成物本身,所記載之用途對於判斷其是否符合新穎性不生作用。
申請專利之發明為一種以醫藥用途界定之醫藥組成物,若其中具有特定藥理作用之化合物與引證文件中化合物相同,其與先前技術之差異僅在於二者之醫藥用途不同,則申請專利之發明不具新穎性。例如,申請專利之發明為「一種用於治療疾病Z之醫藥組成物,其包含有效量之化合物A」,先前技術揭露「一種用於治療疾病X之醫藥組成物,其包含有效量之化合物A」,二者均包含相同之化合物A,雖然治療疾病Z與治療疾病X為不同之醫藥用途,惟決定其本質特性之成分及組成並未改變,故申請專利之發明不具新穎性。惟若將申請專利之發明修正為醫藥用途請求項,例如「一種化合物A之用途,其係用於製備治療疾病Z之醫藥組成物」,因先前技術未揭露化合物A具有治療疾病Z之醫藥用途,則申請專利之發明相較於先前技術具有新穎性。
例1.
[申請專利範圍]
一種錠劑,其包含有效量之A化合物。
[說明]
引證文件揭露一種注射劑,該注射劑包含有效量之A化合物,雖引證文件已揭露A化合物,惟錠劑與注射劑屬不同之劑型,適用於錠劑及注射劑之賦形劑(例如填充劑等)亦不相同,故所請之錠劑具有新穎性。
5.2.3醫藥用途
若化合物或組成物具有新穎性,其醫藥用途請求項當然具有新穎性;例如化合物A具有新穎性,則「化合物A用於製備治療疾病B藥物之用途」當然具有新穎性。若化合物或組成物不具新穎性,其醫藥用途請求項是否具有新穎性係就所使用之化合物或組成物所主張的醫藥用途來判斷,例如組成物B不具新穎性,則「一種醫藥組成物B之用途,其係用於製備治療疾病X之藥物」是否具有新穎性,係就組成物B於治療疾病X之用途是否具有新穎性來判斷。
醫藥用途請求項之醫藥用途通常係指所適用之病症名稱或藥理作用,惟若發明之技術特徵係針對已知組成物用於已知病症或藥理作用,另提出新的治療應用,例如特定患者群、特定部位、使用劑量、給藥途徑、給藥間隔及不同成分先後服用等技術特徵,只要其中任一技術特徵能與先前技術明確區分,則該醫藥用途請求項具有新穎性。
以引證文件核駁某化合物或組成物之醫藥用途的新穎性時,引證文件關於該醫藥用途之記載,通常必須達到充分揭露而可據以實現之程度,例如申請專利之發明為「一種醫藥組成物B之用途,其係用於製備治療疾病X之藥物」,而引證文件揭露該組成物B可用於治療疾病X,且揭露之相關試驗結果足以證明組成物B可用於治療疾病X,則引證文件可證明申請專利之發明不具新穎性,反之,若引證文件之相關試驗結果僅揭露組成物B之特定活性與疾病X之關聯性,且該發明所屬技術領域中具有通常知識者依據該關聯性無法確認組成物B可治療疾病X,或該試驗結果僅能代表組成物B具有安全性(例如以受試者為健康志願者之人體第I期臨床試驗結果),則引證文件無法證明申請專利之發明不具新穎性。一般而言,試管內或以動物模式進行的藥理效果或觀察而得之行為效果,若對該發明所屬技術領域中具有通常知識者而言,可直接且無歧異地得知該醫藥用途者,均足以作為證明其醫藥用途不具新穎性的證據。原則上,審查人員可使用陳述該化合物或組成物用於治療特定疾病但未描述確實的臨床數據之引證文件來核駁其新穎性,然而須注意該文件之陳述是否達到充分揭露而可據以實現之程度。
考量是否屬於不同之醫藥用途應注意:
(1)即使申請專利之醫藥用途與引證文件揭露之醫藥用途表現方式不同,惟考量申請時之通常知識,申請專利之醫藥用途若有下列任一種情形時,仍不具新穎性:
(i) 申請專利之醫藥用途係由引證文件揭露之醫藥用途的相同藥理作用直接且無歧異導出。例如引證文件揭露製備支氣管擴張劑的用途,申請專利之醫藥用途揭露製備氣喘治療劑的用途;引證文件揭露製備血管擴張劑的用途,申請專利之醫藥用途揭露製備降血壓劑的用途;引證文件揭露製備組織胺H2受體抑制劑的用途,申請專利之醫藥用途揭露製備胃潰瘍治療劑的用途等。
(ii)申請專利之醫藥用途係不可避免地由密切相關的藥理效果所產生。例如引證文件揭露製備強心劑的用途,申請專利之醫藥用途揭露製備利尿劑的用途;引證文件揭露製備消炎劑的用途,申請專利之醫藥用途揭露製備鎮痛劑的用途。
(2) 申請專利之醫藥用途為上位概念發明,引證文件所揭露之醫藥用途是申請專利之發明的下位概念發明時,申請專利之醫藥用途不具新穎性。例如,引證文件揭露製備抗精神病劑的用途,申請專利之醫藥用途揭露製備中樞神經作用劑的用途;引證文件揭露製備肺癌治療劑的用途,申請專利之醫藥用途揭露製備抗癌劑的用途。
(3) 於引證文件揭露之醫藥用途,若申請專利之醫藥用途係發現該引證文件揭露之醫藥用途的藥理作用,而主張其為新的醫藥用途,且該二種用途是實質上不可區分者,則申請專利之醫藥用途不具新穎性。例如引證文件揭露一種製備抗菌劑的用途,申請專利之醫藥用途揭露一種製備細菌細胞膜形成之抑制劑的用途。
5.2.4案例
例1. 新醫藥用途
[申請專利範圍]
一種化合物A於製備治療阿茲海默症藥物之用途。
[說明]
說明書揭露已知具有抗菌效果之化合物A係可逆地抑制乙醯膽鹼酯酶(acetylcholine esterase),以防止乙醯膽鹼降解,實施例之藥理試驗結果顯示化合物A具有優異之乙醯膽鹼酯酶的抑制活性及可減少阿茲海默症之症狀。
引證1揭露化合物A具有抗菌效果,但未揭露其具有治療阿茲海默症之功效。另外,無任何先前技術揭露化合物A與具有乙醯膽鹼酯酶抑制活性的化合物之間的結構相似性,亦未揭露化合物A作為抗菌劑之作用機制與治療阿茲海默症的之間的關聯性。
[結論]
請求項所請化合物A用於治療阿茲海默症之用途與引證1揭露化合物A用於抗菌之用途不同,故具有新穎性。
例2. 特定患者族群
[申請專利範圍]
一種化合物X於製備治療乳癌藥物之用途,其中乳癌患者先前接受過芳香酶抑制劑(aromatase inhibitor)及泰莫西芬(tamoxifen)治療失敗。
[說明]
引證1揭露化合物X係為乳癌患者接受泰莫西芬治療失敗後之第二線用藥,且該發明所屬技術領域中具有通常知識者可瞭解乳癌患者對泰莫西芬或對芳香酶抑制劑及泰莫西芬均產生抗藥性之癌細胞的生理特徵並不相同。
說明書揭露針對經過第一線治療藥物泰莫西芬以及第二線治療藥物芳香酶抑制劑治療失敗後之乳癌患者,投予化合物X可有效控制腫瘤。
[結論]
乳癌患者之癌細胞對泰莫西芬產生抗藥性而導致該癌細胞生理特徵改變,另乳癌患者之癌細胞對芳香酶抑制劑及泰莫西芬產生抗藥性亦會導致該癌細胞生理特徵改變,由於產生抗藥性之藥物不同,兩者癌細胞生理特徵之改變亦不同,故請求項所請醫藥用途之患者族群與引證1之患者族群不同,請求項具有新穎性。
例3. 新使用劑量
[申請專利範圍]
一種化合物A於製備治療氣喘藥物之用途,該化合物A以30-40 µg/kg體重劑量,每3個月口服投予至人類。
[說明]
引證1揭露每天口服投予1 µg/kg體重劑量之化合物A至氣喘病人,可減少氣喘之症狀,然而,只要停止投予化合物A,氣喘就會復發,因此,持續不斷地投予化合物A是必要的(每天口服投予1 µg/kg體重劑量之化合物A),惟容易產生副作用B。
說明書揭露每3個月口服30-40 µg/kg體重劑量之化合物A可長時間降低氣喘之症狀,而且大幅降低副作用B發生之機率。
[結論]
由於引證1未揭露以每3個月30-40 µg/kg體重劑量之化合物A來治療氣喘,故請求項所請醫藥用途之使用劑量與給藥方式與引證1不同,請求項具有新穎性。
例4. 新給藥途徑
[申請專利範圍]
一種包含化合物A之組成物於製備治療卵巢癌藥物之用途,其中該化合物A係以100 – 120 µg/kg體重劑量投予至患者腦部之Z部位。
[說明]
引證1揭露包含化合物A之藥物可透過靜脈注射而抑制卵巢癌,但會產生肝毒性之副作用。
說明書揭露將化合物A投予至腦部之Z部位可影響腦下垂體對於賀爾蒙Y之分泌,進而可抑制卵巢癌,且其治療效果相較於已知靜脈注射之給藥途徑有顯著之差異。
[結論]
引證1僅揭露靜脈注射化合物A可抑制卵巢癌之生長,未揭露以包含化合物A的醫藥組成物投予至患者腦部之Z部位可治療卵巢癌,故請求項所請醫藥用途之給藥途徑與引證1不同,請求項具有新穎性。
例5. 給藥間隔
[申請專利範圍]
一種化合物B於製備治療多發性骨髓瘤藥物之用途,該藥物係週期性投予,其中一週期包含投予該化合物B連續21天,接著停藥7天。
[說明]
引證1揭露化合物B可治療多發性骨髓瘤,但未揭露使用週期間隔給藥的方式。
說明書揭露化合物B可週期性投予,其中一週期包含投予化合物B 連續21天,接著停藥7天,可獲得良好治療效果,且可降低副作用產生。
[結論]
引證1未揭露所請醫藥用途請求項之特定給藥間隔,故所請醫藥用途請求項具有新穎性。
5.2.5審查注意事項
申請專利之發明為一種用於治療Y疾病之套組、包裝,其中含有作為活性成分之化合物X以及用法說明書(instruction)(或指示、使用說明書或給藥說明書)。若化合物X用於治療Y疾病之醫藥用途係已知,且此請求項之內容與先前技術的唯一差別僅在於該用法說明書,由於該用法說明書僅為資訊之呈現,對於套組、包裝之結構或組成並無影響,無法使申請專利之發明與先前技術有所區分,故申請專利之發明不具新穎性。
5.3進步性
5.3.1化合物
若申請專利之化合物的結構與已知化合物結構不類似,則不論其是否有無法預期的功效,該化合物具有進步性。
若申請專利之化合物的結構與已知化合物類似且與該已知化合物具有類似用途,因該發明所屬技術領域中具有通常知識者,於該發明申請時能預期到結構類似的化合物具有類似的性質,原則上,該化合物不具進步性。惟若申請專利之化合物具有無法預期的功效,原則上具有進步性。此無法預期的功效可以是與該已知化合物不同的用途,或是較已知化合物之相同用途具有更優異的效果。
5.3.1.1結構類似性之判斷原則
判斷二種化合物的結構是否類似,主要係考量分子結構本身是否具有相同的基本核心部分或基本的環結構。化合物結構相近的程度遞減的順序是:酸及鹼的鹽類、幾何異構物(geometrical isomers)、位置異構物(position isomers)(於相同原子之不同位置具有相同的取代基)、同系物(homologues)(化合物之不同處在於規則地連續加入相同取代官能基團,例如伸烷基-CH2-)。
二種化合物結構上是否類似,亦與所屬技術領域有關,審查時應斟酌不同領域之特性,不能單純由分子結構推定請求之化合物與已知化合物結構是否類似,還必須考量所屬技術領域、結構與效果的關係、應用範圍等多種因素,原則上,化合物結構及效果之關係越密切,則對結構類似之判斷標準應越寬鬆。
5.3.1.2對映異構物
申請專利之發明為一種已知化合物之對映異構物(enantiomer),引證文件已公開該化合物之外消旋混合物(racemic mixture),雖未具體公開至該發明所屬技術領域中具有通常知識者能製造各種光學異構物之程度,惟因具有不對稱碳原子之化合物一般應存在光學異構物,係該發明所屬技術領域之通常知識,且對映異構物通常具有顯著的生物活性亦為可預期者,因此,該發明所屬技術領域中具有通常知識者通常會嘗試使用一般分離或解析異構物之方法,從外消旋物混合物中分離出對映異構物,原則上,該對映異構物不具進步性。除非申請人可證明利用申請時的通常知識無法輕易製得該對映異構物或是請求之對映異構物具有無法預期之功效。
5.3.1.3化合物多晶型
申請專利之發明為一種已知化合物的多晶型,因多晶型的分子結構係與該化合物完全相同,僅結晶型態有所不同,且該發明所屬技術領域中具有通常知識者為解決醫藥領域習知的問題,例如尋求生體可用率(Bioavailability)、安定性更高或溶解度等性質更佳之化合物來製備藥物,有動機進行多晶型的篩選。再者,多晶型通常以例行之實驗方法即可獲得,故原則上已知化合物之多晶型不具進步性,除非該多晶型較該已知化合物具有無法預期之功效。此外,若引證文件已公開一種已知化合物的多晶型A型,申請專利之發明為該化合物的另一種多晶型B型,判斷該發明是否具有進步性通常須考慮先前技術是否已預期有另一種多晶型之存在、該發明所屬技術領域中具有通常知識者是否有動機嘗試製備該多晶型以及是否已瞭解如何製備另一種多晶型,該多晶型是否具有與另一多晶型不同或增進之性質(例如生體可用率、安定性等)等因素。
例1.
引證文件:化合物1a

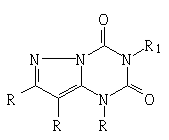 |
申請專利之發明:化合物1b
〔說明〕
結構類似的化合物必須具有相同的基本核心部分或者基本的環,申請專利之化合物1b與引證文件揭露之化合物1a結構不類似,因此具有進步性。
例2.
引證文件:化合物2a H2N-C6H4-SO2NHR1
申請專利之發明:化合物2b H2N-C6H4-SO2-NHCONHR1
〔說明〕
引證文件揭露化合物2a磺胺係用於抗菌,申請專利之化合物2b磺醯脲係用於治療糖尿病,該二個化合物結構雖然類似,但藥理作用不同,申請專利之化合物2b具有進步性。
例3.
引證文件:化合物3a
 |
申請專利之發明:化合物3b
 |
〔說明〕
引證文件揭露之化合物3a與申請專利之化合物3b結構類似,且均具有相同的抑菌功效,但二者同以0.002%濃度使用3天後,引證文件化合物3a之抑菌功效為30%,申請專利之化合物3b之抑菌功效卻達90%,該抑菌功效對於該發明所屬技術領域中具有通常知識者而言,係該發明申請時無法預期者,因此具有進步性。
例4.
引證文件:化合物4a
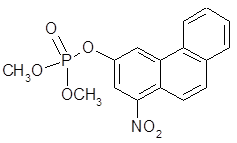
申請專利之發明:化合物4b
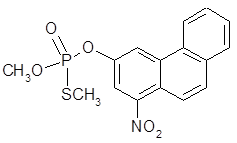
〔說明〕
引證文件揭露之化合物4a與申請專利之化合物4b結構類似,只有SCH3與OCH3之區別,且該發明整體對照先前技術未產生無法預期之功效,不具進步性。
5.3.1.4水合物
申請專利之發明為一種已知化合物之特定含水數的水合物。對於醫藥產物而言,不同含水數對藥物之溶解度、溶解速度及生體可用率、製劑之化學安定性及物理安定性等均有影響,若該發明所屬技術領域中具有通常知識者於確認或預期該化合物有水合物存在之情況下,有動機尋找較佳含水數,並以例行之實驗方法即可獲得該較佳含水數之水合物,則原則上該已知化合物之水合物發明不具進步性,除非申請人能提供請求之水合物具有無法預期功效的證據或其他理由足以證明請求之水合物具有進步性。
5.3.1.5化合物之選擇發明
選擇發明之申請標的與先前技術之差異在於其係從先前技術已知較大的群組或範圍中,選擇其中未特定揭露之個別成分、次群組或次範圍之發明。若該選擇發明未特定揭露於先前技術中,且該選擇發明之全部範圍相較於先前技術均具有無法預期之功效,應認定該發明非能被輕易完成,具有進步性,其他規定另參照第三章3.5「選擇發明之進步性判斷」。
(1)選擇發明不具進步性者
若申請專利之發明僅係由已揭露之廣泛範圍的化合物中選出特定之少數化合物,且未具有無法預期之功效,則不具進步性。例如先前技術揭露以一通式界定之化合物,該通式包括以R表示的取代基,該R取代基之範圍涵蓋廣泛定義的基團,如經鹵素或羥基取代或未經取代之烷基或芳基,但該先前技術僅揭露少數具體實施例。申請專利之發明與該先前技術之差異在於,所請化合物之取代基R係由先前技術揭露之R取代基的廣泛範圍中所選出之具體特定基團,例如芳基,惟先前技術並未具體揭露R取代基為芳基之化合物。若該選擇所生成化合物相較於先前技術之化合物不具有無法預期之功效,或者這些化合物雖具有優於先前技術中明確揭露之化合物的性質或效果,惟該發明所屬技術領域中具有通常知識者於申請時可預期此類化合物具有該性質或效果,而可能會被引導進行這種選擇,則申請專利之發明不具進步性。
(2)選擇發明具有進步性者
若申請專利之發明係由已揭露之廣泛範圍的化合物中選出特定之少數化合物,且具有無法預期之功效,則具有進步性。如上述(1)之經取代化合物,申請專利之發明亦係由先前技術已定義的取代基R之廣泛範圍中選擇特定之芳基,若該選擇所生成化合物較先前技術之化合物具有無法預期之功效,且先前技術並無任何教示或建議引導該發明所屬技術領域中具有通常知識者為了獲得該功效,進行該特定選擇而非其他選擇,則申請專利之發明具有進步性。
5.3.2醫藥組成物
5.3.2.1人類以外的動物用醫藥與人類用醫藥之轉用
申請專利之發明僅將引證文件中已知用於非人類動物之醫藥組成物轉用為人類醫藥組成物,若二者係使用於相同或類似疾病之治療,即使引證文件中並未建議此轉用,原則上申請專利之發明不具進步性,除非申請人能提供該發明具有無法預期之功效等證據或其他理由足以證明其具有進步性。
5.3.2.2組合二個以上成分之組成物
申請專利之組成物是由二個以上之已知成分所界定,若該等成分之組合是新穎且產生無法預期之功效,則申請專利之發明具有進步性。
然而,若二個以上成分組合所成之組成物係該發明所屬技術領域中具有通常知識者,為解決醫藥領域習知之問題,例如增加醫療效果或降低副作用,而會嘗試尋找二個以上成分的最佳組合且經由一般例行工作即可獲得,則申請專利之發明不具進步性。
該等組合例示如下:
(1)已知成分的組合,該等成分之主要作用是相同的,例如針對相同病症具相同治療作用之已知成分的組合。
(2)將已知具有副作用的主要成分與已知可消除該副作用的次要成分組合在一起。例如申請專利之發明為一種醫藥組成物於製備治療腫瘤藥物之用途,該醫藥組成物包含紫杉醇(paclitaxel)以及一種化合物X。已知紫杉醇可用於治療腫瘤,惟投予時會發生嘔吐副作用;又化合物X具有減弱一般性嘔吐之功效亦為已知,因此,為減弱紫杉醇所引發之嘔吐副作用,該發明所屬技術領域中具有通常知識者有動機將紫杉醇與化合物X組合使用,且可預期其治療效果,故申請專利之發明不具進步性。
(3)將具有針對由一主要疾病引起的各種症狀有相對治療效果之已知成分組合在一起。例如申請專利之發明為一種醫藥組成物於製備治療AIDS藥物之用途,其中包括AZT及化合物Z。已知AZT可用於治療AIDS且化合物Z可用於治療肺炎。又該發明申請時已知AIDS會伴隨引發肺炎,因此,在治療AIDS的患者時,為處理因AIDS所引發的肺炎,該發明所屬技術領域中具有通常知識者有動機將AZT及化合物Z組合使用,且可預期其治療效果,故申請專利之發明不具進步性。
例1.
〔申請專利範圍〕
一種治療糖尿病醫藥組成物,其包含重量比為5:1~4:1之化合物A及化合物B。
〔說明〕
化合物A及化合物B為已知之治療糖尿病之藥物。惟單獨服用化合物A會產生體重增加之副作用,此外,並無任何先前技術揭露化合物A及化合物B之組合使用。申請專利之發明係將化合物A及化合物B以特定比例予以組合使用,實施例證實該特定比例之組合能降低化合物A所產生之副作用。
〔結論〕
申請專利之發明與引證1之差異在於引證1未揭露將化合物A及化合物B以特定比例予以組合使用,說明書之藥理試驗結果顯示特定比例之化合物A及化合物B的組合可降低化合物A之副作用,且該功效非該發明所屬技術領域中具有通常知識者於申請時所能預期者,申請專利之發明具有進步性。
5.3.2.3醫藥組合、包裝及套組
有關組合、套組或包裝之進步性,若其與先前技術有差異之技術特徵僅在於不同成分之組合,其判斷原則與5.3.2.2「組合二個以上的成分之組成物」之規定相同。
若組合發明中兩種(或多種)成分具有相乘效果(synergistic effect),原則上該請求項具有進步性;惟若此種組合對該發明所屬技術領域中具有通常知識者而言是顯而易知,且所產生之相乘效果亦為可預期者,該組合仍不具進步性。例如已知止痛劑(analgesic)類活性劑及去充血劑(decongestant)類活性劑可組合使用,申請專利之發明的特徵僅在於從止痛劑及去充血劑中各選出一個成分而形成一個新穎的且更有效之組合,因產生之有利功效為所屬技術領域中具有通常知識者於申請時可預期的,故此種組合不具進步性。
5.3.3醫藥用途
原則上,醫藥用途的進步性判斷方式係就所使用之化合物等活性成分及所主張的醫藥用途來判斷,醫藥用途通常係指所適用之病症名稱或藥理作用,惟若發明之技術特徵係針對已知組成物用於已知病症或藥理作用,提出新的治療應用,例如特定患者群、使用劑量、給藥途徑、給藥間隔、不同成分先後服用等技術特徵,則須考量包含該技術特徵之發明的整體相較於先前技術是否具進步性。
為解決醫藥領域中具有通常知識者習知的問題,例如增加醫療效果或減少副作用,尋找使用劑量、給藥間隔、給藥途徑等醫藥使用方式的最佳條件,若為該發明所屬技術領域中具有通常知識者經由一般例行性工作即可獲得,且其功效是該發明所屬技術領域中具有通常知識者能夠預期者,則不具進步性。除非申請人能提供該發明具有無法預期之功效等證據或其他理由足以證明其具有進步性。
再者,雖然申請專利之醫藥用途與引證文件揭露的醫藥用途內容不同,但是由申請時之通常知識可推導出兩者之作用機制的關連性,原則上,申請專利之醫藥用途不具進步性,除非申請人能提供該發明具有無法預期之功效等證據或其他理由足以證明其具有進步性。
5.3.4案例
例1. 使用劑量(一)
〔申請專利範圍〕
一種膠原蛋白酶(collagenase)之用途,其係用於製備治療疾病X之藥物,該藥物為包含至少10,000單位膠原蛋白酶之可供局部注射單一劑量,且其濃度為每毫升20,000至40,000單位。
〔說明〕
說明書揭露以該高濃度局部注射高單一劑量之膠原蛋白酶,對於多次以較低濃度注射相同總劑量而無效之患者,能給予安全且有效之治療。
引證1揭露膠原蛋白酶可用於治療疾病X,惟其使用濃度遠低於請求項所界定範圍,且須多次注射。
〔結論〕
申請專利之發明與引證1之差異在於以局部注射高濃度之膠原蛋白酶來治療疾病X,惟因局部注射高濃度之膠原蛋白酶會對局部組織產生傷害係申請時之通常知識,該發明所屬技術領域中具有通常知識者於申請時應無動機嘗試以高濃度之膠原蛋白酶溶液施予局部注射,且預期能安全有效地治療疾病X,故申請專利之發明並非該發明所屬技術領域中具有通常知識者依申請前之先前技術所能輕易完成者,具有進步性。
例2. 使用劑量(二)
〔申請專利範圍〕
一種化合物A於製備鎮咳藥物之用途,其使用劑量為口服400 ~ 450 µg/kg體重,1天1次。
〔說明〕
說明書實施例為口服400 µg/kg體重,1天1次,顯示止咳效果增加。
引證1揭露鎮咳用之化合物A的使用劑量為口服160 µg/kg體重,1天3次。
〔結論〕
申請專利之發明與引證1之差異在於提高化合物A用於鎮咳之使用劑量,但減少給藥次數,惟為解決醫藥所屬技術領域之習知的問題,例如提升藥效、增進服藥順服性等而調整藥物之適當劑量或使用頻率,係該發明所屬技術領域中具有通常知識者經由一般例行性工作即可獲得,且其功效係該發明所屬技術領域中具有通常知識者於該發明申請時所能預期者,故申請專利之發明係引證1揭露之劑量的簡單變更,為該發明所屬技術領域中具有通常知識者依申請前之先前技術所能輕易完成者,不具進步性。
例3. 特定患者族群
〔申請專利範圍〕
一種化合物X於製備治療乳癌藥物之用途,其中乳癌患者先前接受過泰莫西芬(tamoxifen)及芳香酶抑制劑(aromatase inhibitor)治療失敗。
〔說明〕
說明書揭露針對經過第一線治療藥物泰莫西芬以及第二線治療藥物芳香酶抑制劑治療失敗後之乳癌患者,投予化合物X可有效控制腫瘤。
引證1揭露化合物X可作為乳癌患者之第二線治療藥物,其與泰莫西芬均為雌激素受體(estrogen receptor)調節劑。
〔結論〕
申請專利之發明與引證1之差異在於化合物X用於治療乳癌之患者群不同,雖然引證1揭露化合物X可作為乳癌患者之第二線治療藥物,惟對產生抗藥性之腫瘤而言,其生理或病理特徵(physiological or pathological characteristics)已產生改變,該發明所屬技術領域中具有通常知識者無法預期其能作為第三線治療藥物,而對經泰莫西芬與芳香酶抑制劑治療失敗之乳癌患者有效,此外,化合物X之藥理作用與泰莫西芬相近,對於該發明所屬技術領域具通常知識者而言,無動機選擇藥理作用相近藥物作為後線之治療藥物,故申請專利之發明並非該發明所屬技術領域中具有通常知識者依申請前之先前技術所能輕易完成者,具有進步性。
例4. 藥理作用之關聯性
〔申請專利範圍〕
一種化合物A於製備治療非酒精性脂肪肝病(NAFLD)藥物之用途。
〔說明〕
說明書揭露化合物A具有改善非酒精性脂肪肝病之功效。
引證1揭露化合物A可增進胰島素敏感性,用於治療糖尿病,其作用機制係活化受體X,又引證2揭露藉由活化受體X能治療非酒精性脂肪肝病。
〔結論〕
申請專利之發明與引證1之差異在於,引證1揭露化合物A為受體X之激動劑,可增進胰島素敏感性而治療糖尿病,但未揭露其可用於治療非酒精性脂肪肝病,惟引證2已揭露活化受體X能調節肝臟脂肪之代謝與分布,進一步改善非酒精性脂肪肝病,由於引證1及2均屬於「活化受體X」之相關技術領域,且引證1揭露化合物A為受體X之激動劑,引證2揭露活化受體X能改善非酒精性脂肪肝病,二者具有功能或作用的共通性。因此,該發明所屬技術領域中具有通常知識者有動機結合引證1及2之技術內容,而輕易完成申請專利之發明,故不具進步性。
例5. 治療具共同致病因素之疾病
〔申請專利範圍〕
一種異戊二烯基甲酮化合物於製備抗胃炎藥物之用途。
〔說明〕
說明書揭露已知異戊二烯基甲酮化合物之新醫療用途,申請人主張胃炎和胃潰瘍是二種不同的疾病。引證1揭露使用異戊二烯基甲酮化合物治療胃潰瘍,且其藥理作用係保護胃黏膜以及抗引發胃炎之侵犯因子。
〔結論〕
申請專利之發明與引證1之差異在於異戊二烯基甲酮化合物用於治療的疾病不同,惟胃炎及胃潰瘍雖然是二種不同的疾病,但是二者具有共同的致病因素(causative factors),例如胃部發炎,且使用相同的藥物來治療胃炎及胃潰瘍係屬申請時之通常知識。由於引證1已揭露異戊二烯基甲酮化合物可用於治療胃潰瘍,該發明所屬技術領域中具有通常知識者依據引證1之內容及申請時之通常知識可合理推論異戊二烯基甲酮化合物也可用於治療胃炎,故申請專利之發明係引證1揭露之疾病的簡單變更,為該發明所屬技術領域中具有通常知識者依申請前之先前技術所能輕易完成者,不具進步性。
6.發明單一性
有關單一性的判斷,應先參照第四章發明單一性之規定。此處說明與醫藥化學相關發明相同或對應的技術特徵之判斷。
6.1化合物請求項
6.1.1馬庫西型式請求項
以馬庫西型式之擇一記載形式界定申請專利範圍時,擇一形式的各個選擇項目(alternatives)具有類似本質(nature)時,則認為各個選擇項目於技術上互相關聯,具有相同或對應的技術特徵。
以馬庫西型式之擇一記載形式界定化合物發明時,判斷其中並列的各選擇項目(即可供選擇之化合物)是否具有類似的本質,應考慮是否同時符合下列條件:
(1)所有選擇項目具有共同的性質或活性;且
(2)(a)所有選擇項目具有共同的結構,亦即所有選擇項目共有一個重要化學結構要素(element),或(b)雖然共同的結構無統一的判斷標準,但所有的選擇項目可被認定屬於該發明所屬技術領域中具有通常知識者「所公認之化合物群」。
上述(2)(a)中之「所有的選擇項目共有一個重要化學結構要素」,係指所有選擇項目都具有一種共同的化學結構,該共同的化學結構佔了其結構的絕大部分,或若該化合物的共同的化學結構只佔了其化學結構的小部分,但以先前技術來看,該共同的結構部分構成了結構上獨特的部分。該化學結構要素可以是單獨之一部分(component),亦可為幾個獨立部分連接而成之組合。
上述(2)(b)之「所公認之化合物群」係指依據該發明所屬技術領域的通常知識,可以預想到該類的成員對於申請專利之發明,係為具有相同作用之同一類化合物群。換言之,屬於此類化合物之各個化合物,都可互相替代而可預期達到相同的結果。
若經檢索發現馬庫西型式請求項中,至少有一個選擇項目已公開於先前技術,即不具有相同或對應之特別技術特徵,則必須重新考量該請求項是否具發明單一性。
例1. 馬庫西型式:共同的結構
〔申請專利範圍〕
一種結構式如下的化合物:
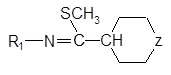
其中R1選自苯基、吡啶基、噻唑基、三嗪基、硫代烷基、烷氧基及甲基;Z選自氧、硫、亞胺基及亞甲基。
〔說明〕
此例中,-N=C-SCH3連接到六員環的結構是所有選擇項目共有的重要結構要素,且對先前技術為有所貢獻之特別技術特徵,而所有請求之化合物都主張可用作舒緩下背痛的藥物之相同功效,故請求項之所有化合物之間具有相同或對應之特別技術特徵,具發明單一性。
例2. 馬庫西型式:無共同的結構
〔申請專利範圍〕
一種如通式所示之的化合物:A-B-C-D-E,其中:
A選自C1-C10烷基或C2-C10烯基或C3-C10環烷基,取代或未取代的芳基或含有1至3個選自O及N雜原子之C5-C7雜環;
B選自C1-C6烷基或C2-C6烯基或C2-C6炔基,氨基,磺基,C3-C8醚或硫醚;
C選自含有1至4個選自O,S或N雜原子之C5-C8飽和或不飽和雜環,或取代或未取代的苯基;
D選自B或C4-C8羧酸酯基或醯胺基;及
E選自取代或未取代的苯基,萘基,茚基,吡啶基或噁唑基。
〔說明〕
由上述通式中不能確定主要結構要素為何,因此所有的選擇項目之間不具有共同的結構,故請求項之所有化合物之間不具相同或對應的技術特徵,明顯不具發明單一性。
6.1.2中間體與最終產物
涉及中間體與最終產物的發明,若同時符合下列(a)及(b)兩個條件,則具有相同或對應技術特徵:
(a)中間體及最終產物具有相同之基本結構要素,即
(i) 中間體及最終產物的基本化學結構相同,或
(ii) 二種產物的化學結構在技術上是密切相關的,該中間體將一個基本結構要素提供給最終產物中,且
(b)中間體及最終產物於技術上互相關聯,即最終產物是直接從中間體製造出來的,或是直接由中間體中分離出來的。
若在同一件申請案,請求製備同一最終產物的不同方法中所用的不同中間體,只要這些中間體具有相同的基本結構要素,即具有相同或對應技術特徵。
若在同一件申請案,請求同一最終產物的不同結構部分之不同中間體,則明顯不具發明單一性。
例1. 中間體/最終產物
〔申請專利範圍〕
1.一種結構式如下的化合物:
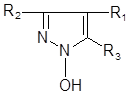
2.一種結構式如下的化合物:
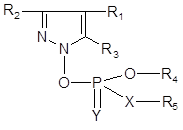
〔說明〕
中間體與最終產物的化學結構存在著技術上的密切相關性,提供給最終產物的基本結構要素是:
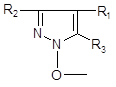
因此,請求項1及2之間具有相同或對應之技術特徵。
6.2醫藥組成物請求項及醫藥用途請求項
醫藥組成物及醫藥用途請求項所界定之醫藥用途若係針對不同種類的疾病,則須注意是否屬於一個廣義發明概念,即具有相同或對應之特別技術特徵,例如請求項所涵蓋之該等病症是彼此相關的(且與請求項所涉之已知的病症無關),或是這些疾病之治療或診斷係屬共通的作用機制,始認定申請專利之發明具有發明單一性。