基因工程間充質幹細胞及其應用
細胞再生、組織修復 基因工程大躍進
近年再生醫學蓬勃發展,相對於幹細胞,外泌體在臨床治療上更安全、有效且排斥風險小。中國醫藥大學團隊開發出強化版外泌體,可有效抑制腦中風引發的免疫反應、修復受損組織及促進神經再生,讓患者恢復自理能力。
根據衛福部統計,腦血管疾病為國人十大死因的第四位,平均每年奪走一萬多條寶貴生命,腦中風即使存活後,仍有50%患者會遺留不同程度的神經功能障礙,造成身心失能。
中國醫藥大學醫療體系執行長鄭隆賓指出,急性腦中風的常規治療除了機械取栓、藥物和復健治療等,隨著再生醫學的蓬勃發展,中國醫藥大學附設醫院已開始運用幹細胞來治療中風後遺症;然而,細胞治療存在細胞培養穩定度保存不易、免疫排斥問題及致瘤性風險,因此新穎的幹細胞衍生治療藥劑「外泌體」(Exosome)便應運而生。
非病毒載體 降低致病風險
外泌體是一種由細胞分泌的微小囊泡,扮演細胞間訊號傳輸的媒介,生物相容性高,尺寸介於30奈米到200奈米之間,可穿過血腦屏障,在臨床治療上被視為具潛力的非細胞治療劑。
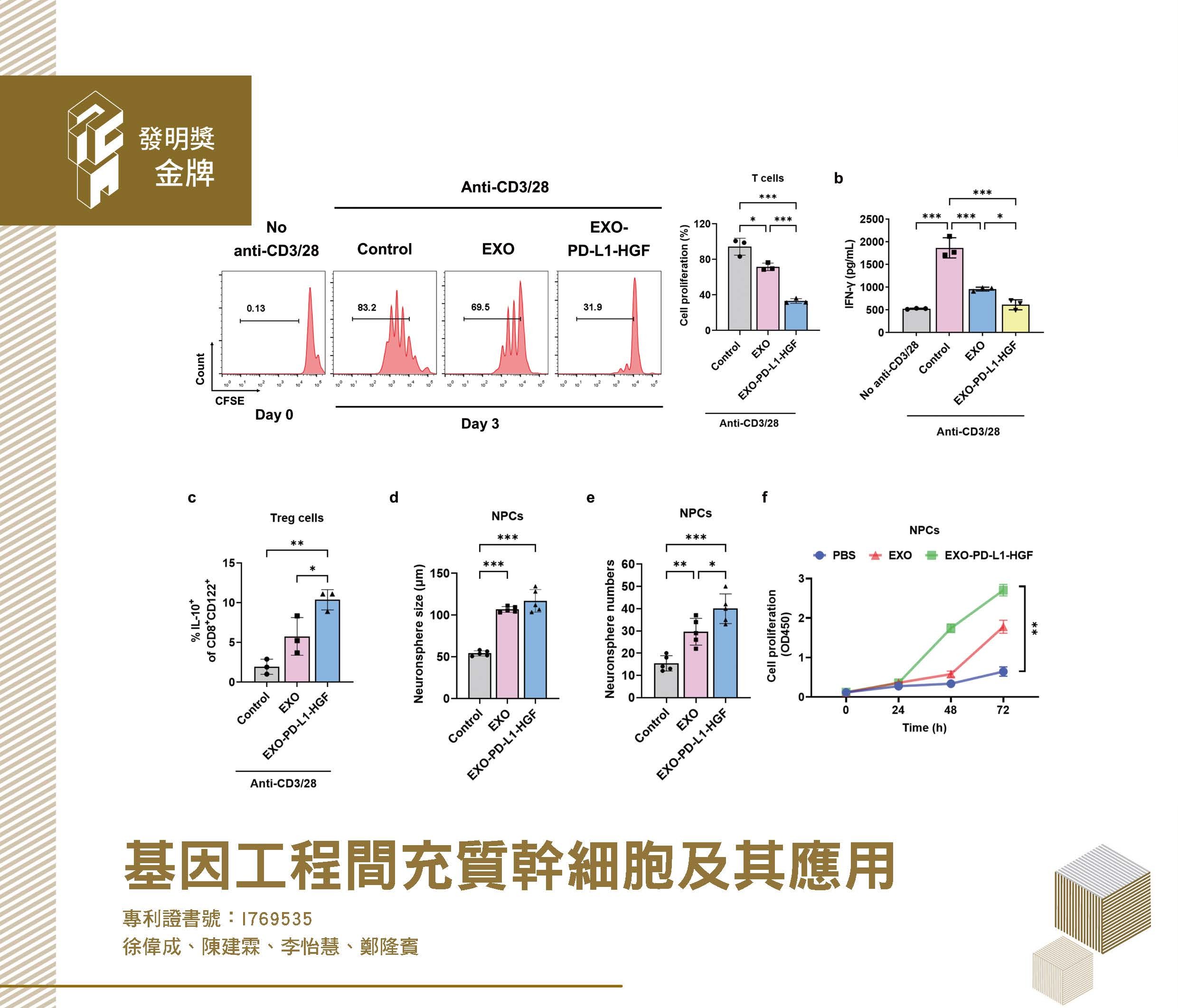
中國醫藥大學附設醫院副院長徐偉成提及,團隊致力開發升級版的異體臍帶間質幹細胞衍生的外泌體(EXO-PD-L1-HGF),首先必須透過特殊的非病毒轉殖的雙基因工程修飾技術,將PD-L1和HGF修飾裝載到間質幹細胞內,再將其衍生的外泌體進行分離純化,然後做動物實驗。整個研究花了近六年時間,於2022年7月取得「基因工程間充質幹細胞及其應用」專利。
鄭隆賓也提及,過程中最大的挑戰是基因傳遞方式,以往都是用病毒載體,但也存在潛在性的危險,因此團隊利用基因工程轉殖技術,將雙基因經由非病毒電轉染方式送進間質幹細胞中,不僅更安全,且具有低免疫原性、高基因負載能力等優點,是重要的技術突破。
雙基因修飾 促進修復再生
相較於無基因修飾的外泌體,EXO-PD-L1-HGF具有抑制發炎反應、抵抗因氧化壓力引起的細胞凋亡、主動標靶功能及促進腦內源性神經幹細胞增生及分化,可大幅提升修復受損組織和神經再生能力。
本專利在研發初期的概念驗證(Proof of Concept, POC)已由基礎實驗室完成,並於動物試驗進行確效試驗;2023年8月技術移轉授權予聖安生醫,之後再授權顥晟生醫,進行後續藥證取得與新藥商品化事宜。
技術再優化 逐步擴大應用
鄭隆賓指出,團隊致力於研究和開發可應用於中風、癲癎、藥物成癃等中樞神經系統疾病的特異性藥物,目前在腦中風治療已見成效,第二階段專注的是急性腎損傷,使用外泌體進行治療,腎功能恢復的效果更加顯著;此外,外泌體也可修復心肌梗塞造成的心肌受損,以及在治療代謝異常性脂肪肝(MASLD)方面發揮重要作用。同時團隊正在研發下一代轉殖方式,達到更好的治療效益,廣泛應用於疾病診斷與治療,造福更多病人。
- 發布日期:114-08-15
- 更新日期: 114-08-15
- 發布單位:專利行政企劃組
- 點閱次數:835

